Tabla de Contenidos
Examen Parcial - 63.11. Química Aplicada A - 13/10/2000
Cátedra: Todas
Fecha: 1º Oportunidad - 2º Cuatrimestre - 2000
Día: 13/10/2000
Enunciado
- Calcular para un mol de nitrógeno gaseoso a
 y
y  , considerado como gas ideal en ese intervalo de temperaturas, relativo a la condición standard:
, considerado como gas ideal en ese intervalo de temperaturas, relativo a la condición standard:
a) ; b)
; b) ;
;  ;
;  ;
; 
Datos: ;
;  ;
; 
- Para la reacción:
 , la energía libre de reacción en
, la energía libre de reacción en  , como función de la temperatura
, como función de la temperatura  , puede representarse por las siguientes relaciones empíricas:
, puede representarse por las siguientes relaciones empíricas:
i)
ii)
iii)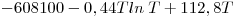
Dependiendo solamente del estado de agregación del magnesio (sólido, líquido, gaseoso): a) indicar que ecuación corresponde a cada caso. Fundamentar la respuesta. Sin resolver númericamente plantear las ecuaciones para calcular: b) T de fusión y c) la T de ebullición normal (las respuestas deben contener solo constantes y la varaiable a calcular). - a) Calcular
 y
y  para la disociación del
para la disociación del  a
a  . Indicar las aproximaciones que sean necesarias.
. Indicar las aproximaciones que sean necesarias.
b)Calcular el grado de disociación del a
a  y a
y a  .
.
Datos: ;
;  ;
;  ;
; 
Para la reacción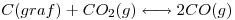
![<tex>T[^{\circ}C]</tex> <tex>T[^{\circ}C]</tex>](lib/plugins/latex/images/34f4742f380c97c2ffa357d60d5c659879e7c738_0.png) | ![<tex>P_t[atm]^{\circ}</tex> <tex>P_t[atm]^{\circ}</tex>](lib/plugins/latex/images/682ea52dae8df8f16fe2e15beecc7da027f5cbac_0.png) | 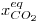 |
| 800 | 2,3 | 0,7455 |
| 900 | 2,3 | 0,9308 |
- 4. Calcular la concentración de todas las especies en equilibrio en una solución 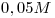 de ácido monocloroacético
de ácido monocloroacético 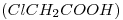 antes y después del agregado de
antes y después del agregado de 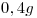 de
de 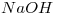 sólido a un litro de solución. Considere desestimable la variación de volúmen por el agregado de sólido.
sólido a un litro de solución. Considere desestimable la variación de volúmen por el agregado de sólido.
Datos: 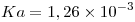 ;
; 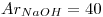
Resolución
Esta página está incompleta; podés ayudar completando el material.
Discusión
No puedo centrar la tabla del punto 3. Y Tampoco puedo lograr que aparezca la numeración en el ejercicio 4.
Excepto donde se indique lo contrario, el contenido de esta wiki se autoriza bajo la siguiente licencia: CC Attribution-Noncommercial-Share Alike 3.0 Unported
