Tabla de Contenidos
Exámen Parcial - 63.01. Química 1
Cátedra: Olezza
Fecha: 2ª Oportunidad - 2º Cuatrimestre 2002
Día: xx/10/2002
Esta página está incompleta; podés ayudar completando el material.
Enunciado
Parte A
Indicar si las siguientes aseveraciones son verdaderas o falsas y justificar brevemente su respuesta.
- Hay una energía mínima para iniciar cualquier transformación química.
- Expresar la concentración del soluto como molaridad o malalidad no tiene ninguna influencia (no afecta) en el calculo de ascenso ebulloscopico.
- El calor de disolución al formarse una solución ideal es cero
- La temperatura es una medida de la energía media de las moléculas de un gas
- Durante la compresión isotérmica de un vapor la presión se mantiene siempre constante.
- En las ecuaciones termoquímicas debe especificarse el estado de agregación de las sustancias participantes.
- En una solución ideal que presenta desviaciones positivas:
- La presión de vapor de la solución medida es inferior a la calculada a través de la Ley de Raoult
- Las fuerzas de interacción entre las moléculas de soluto y solvente son iguales a las que existen entre las moléculas del solvente entre si y las moléculas del soluto entre sí
Problema 1
Calcule la entalpía molar de combustión a 298K de la glicina 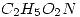 , una sustancia importante para la energía biológica, sabiendo que en dicha reacción se produce dióxido de carbono, agua y nitrógeno gaseoso, conociendo las entalpías molares estandar de formación a la misma temperatura.
, una sustancia importante para la energía biológica, sabiendo que en dicha reacción se produce dióxido de carbono, agua y nitrógeno gaseoso, conociendo las entalpías molares estandar de formación a la misma temperatura.
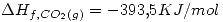
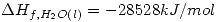
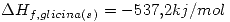
Escribir todas las ecuaciones termoquímicas y aplicar las leyes de Hess
Si reaccionan 10g de glicina cual es el calor intercambiado; Calcular W y ΔE
Problema 2
- Se coloca 1ml de ácido sulfúrico concentrado (25% densidad=1.18 g/ml) en un matraz de 500ml y se diluye con agua hasta completar el volumen. Se toman 20ml de la solución así preparada y se vierten en un erlenmeyer al cual se le agregan 25ml de agua. ¿qué volumen de hidróxido de sodio 0.100M se necesita para neutralizar el ácido contenido en el Erlenmeyer? ¿cuál era la concentración expresada en mol/l del ácido concentrado original?
- La reacción de neutralización del item anterior es exo o endotérmico, justificar.
- Si en lugar de neutralizar con hidróxido de sodio se realiza la determinación con hidróxido de calcio de la misma molaridad se consume menos, igual o más volumen de solución.
Problema 3
- Calcule la altura de la altura de la columna final de agua que mediria en un aparato armado como en la experiencia de determinación de masa molar de Mg si los datos obtenidos son los siguientes: m Mg=0.05g P=750mmHg T=30°C Pv=31.82mmHg Vhidrogenno=52ml y densidadHg=13.6g/ml
- ¿Qué entiende por solución diluida?, marquen en una curva de solubilidad a la misma temperatura una solución diluida y una sobresaturada.
- ¿Cuál puede ser una causa de error en la determinación de la atomicidad del azufre?. Justifique
Discusión
Si ves algo que te parece incorrecto en la resolución y no te animás a cambiarlo, dejá tu comentario acá.
Excepto donde se indique lo contrario, el contenido de esta wiki se autoriza bajo la siguiente licencia: CC Attribution-Noncommercial-Share Alike 3.0 Unported
