Tabla de Contenidos
Parcial segunda parte - 76.45. Termodinámica de los Procesos
Cátedra: Única
Fecha: 1° Oportunidad - (2º Cuatrimestre 2007)
Día: 23/11/2007
Punto 1
Los datos experimentales del calor de mezclado para la mezcla liquida n-octanol (1) /n-decano (2) pueden ajustarse mediante la curva ![<tex>\mathit{H=x _1 \cdot x _2[A+B(x _1 \cdot x _2)]}</tex> <tex>\mathit{H=x _1 \cdot x _2[A+B(x _1 \cdot x _2)]}</tex>](lib/plugins/latex/images/9619d1ba0bb8e8e01b73bad95b63377b764ea0a9_0.png)
Con 
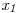 : fracción molar de n-octanol
: fracción molar de n-octanol ![<tex>\mathit{T: [K] \; y \; H:[J/mol]}</tex> <tex>\mathit{T: [K] \; y \; H:[J/mol]}</tex>](lib/plugins/latex/images/a8b75ab82d2f446710bbcb6c429ea7310b519ff8_0.png)
- a) Calcule los valores de la entalpía molar para el n-octanol y el n-decano puros a 300K. ¿qué puede decir de los valores que obtuvo?
- b) Calcule los valores de la entalpía molar parcial para el n-octanol y el n-decano, en la mezcla liquida con concentración 50% molar de n-octanol a 300K.
- c) Se tienen dos soluciones (Sa y Sb) con concentraciones molares en n-octanol del 20% (Sa) y 90% (Sb) respectivamente. Ambas soluciones fluyen en estado estacionario dentro de una cámara de mezclado a 27°C y con una relación de flujos molares:
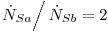
- calcule el flujo de calor por mol de solución que abandona el mezclador [J/mol Sc] necesario para mantener la temperatura de la misma en 300K (
 )
) - ¿Durante el mezclado debería agregarse o quitarse calor?
- d) Grafique
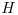 vs.
vs. 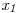 a 300K y muestre la relación entre los valores graficados y los calculados en (b).
a 300K y muestre la relación entre los valores graficados y los calculados en (b). - e) Usando el gráfico estime los valores de la entalpía molar parcial para el n-octanol a dilución infinita y para el n-decano a dilución infinita.
Punto 2
A presión atmosférica, la mezcla acetona (1) / cloroformo (2) forma un azeótropo a 64,6°C, el cual tiene una concentración molar de acetona en la fase líquida del 33,5%. A 64,6°C la presión de saturación de la acetona es 1,31 atmósferas y la del cloroformo 0,98 atmósferas. El comportamiento de la solución liquida puede ser descrito por la ecuación de Van Laar:
![<tex>\mathit{ln \gamma _1= A _{12} \left.[1+(A _{12} \cdot x _{1} \right/ A _{21} \cdot x _2 )] ^{-2}} \qquad \mathit{ln \gamma _2= A _{21} \left.[1+(A _{21} \cdot x _{2} \right/ A _{12} \cdot x _1 )] ^{-2}}</tex> <tex>\mathit{ln \gamma _1= A _{12} \left.[1+(A _{12} \cdot x _{1} \right/ A _{21} \cdot x _2 )] ^{-2}} \qquad \mathit{ln \gamma _2= A _{21} \left.[1+(A _{21} \cdot x _{2} \right/ A _{12} \cdot x _1 )] ^{-2}}</tex>](lib/plugins/latex/images/84f2090dea933b219e4cfaecf22be435d90ab6b7_0.png)
- a) Plantee la forma general de la ecuación que gobierna el equilibrio liquido vapor. Liste la suposiciones que considere adecuadas para este problema. Justifique debidamente cada una de ellas, y halle la ecuación modificada para las condiciones del problema.
- b) Calcule los coeficientes de actividad de la acetona y del cloroformo en el azeótropo.
- c) Determine el valor de la energía libre de Gibbs en exceso, en kcal/kmol, para el azeótropo.
- d) Calcule la presión que se ejerce a 64,6°C sobre una solución liquida de acetona (1) / cloroformo (2) que contiene 12 % molar de acetona. Considere:
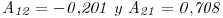
- e) Calcule la composición del vapor en equilibrio con la solución liquida en las condiciones de (d).