Tabla de Contenidos
Examen Final - 63.01. Química B - 06/03/08
Fecha: 5ª oportunidad - Verano 2008
Día: 06/03/2008
Esta página está incompleta; podés ayudar completando el material.
Enunciado
No copié el enunciado formalmente sino un poco taquigraficamente, tal vez en la reescritura se perdieron sutilezas de la redacción. Está invitado cualquiera con una versión más formal a reescribilo. — Sebastián Santisi 2008/03/06 21:58
Punto I
- Se tiene una pila donde un electrodo es de
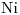 en solución de concentración 10-2M de
en solución de concentración 10-2M de 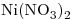 y el otro es de
y el otro es de 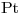 en solución 10-2M de
en solución 10-2M de  a la que se hace llegar
a la que se hace llegar 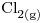 a 10-3atm.
a 10-3atm.- Dar el potencial de cada electrodo y la fem de la pila.
- Escribir las ecuaciones iónicas en cada electrodo y escribir la pila de acuerdo a la notación convencional.
- Se tienen dos celdas electrolíticas conectadas en serie. Tienen 1 litro de solución acuosa de concentración 1M, respectivamente para cada una de: 1)
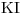 , 2)
, 2) 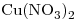 . Por ella circula una corriente de 5A durante 1 hora.
. Por ella circula una corriente de 5A durante 1 hora.- Escribir las ecuaciones de las reacciones en el ánodo y el cátodo de cada cuba.
- Calcular el Ph luego de la electrólisis, despreciando cambios de volumen.
Eran datos: E0 de 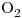 /
/ ,
, 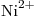 /
/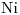 ,
, 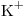 /
/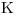 ,
,  /
/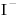 ,
, 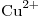 /
/ ,
, 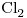 /
/ .
.
Punto II
Se tiene un tanque de hierro, de base cuadrada de 60cm de lado y de 1,5m de altura. Ha habido una corrosión de 0.02mm luego de 6 meses de exposición a la intemperie.
- Escriba la ecuación de la corrosión. Calcule la masa de
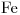 perdida. Calcule la intensidad media de corriente.
perdida. Calcule la intensidad media de corriente. - ¿Qué tipo de protección catódica propondría?; escriba sus ecuaciones.
- Para
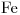 ,
, 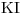 y
y  en estados sólido. ¿Qué tipo de solidos son?; ¿cuáles las particularidades de los nodos de sus celdas unitarias?; ¿qué tipo de fuerzas intervienen?; ¿cuál es su conductividad eléctrica?
en estados sólido. ¿Qué tipo de solidos son?; ¿cuáles las particularidades de los nodos de sus celdas unitarias?; ¿qué tipo de fuerzas intervienen?; ¿cuál es su conductividad eléctrica?
Era dato: 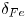 = 7.0g/cm3.
= 7.0g/cm3.
Punto III
- Se tiene una caldera generadora devapor la cual es alimentada con 100Kg de fuel oil (
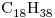 ) por día. Se sabe que la pérdida de calor es del 15% y que la combustión es completa. La presión es de 1atm.
) por día. Se sabe que la pérdida de calor es del 15% y que la combustión es completa. La presión es de 1atm.- Escriba la ecuación de la combustión.
- Calcule la máxima producción de vapor de agua a 100ºC en Kg/h sabiendo que el agua entra a 25ºC.
- Q, W,
 ,
,  en KJ para la situación del punto anterior, por hora.
en KJ para la situación del punto anterior, por hora.
- Eran datos:
 = -4000Kcal/mol,
= -4000Kcal/mol, 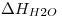 (de vaporización) = 540cal/g,
(de vaporización) = 540cal/g, 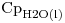 = 1cal/g.
= 1cal/g.
- La caldera anterior es alimentada con agua a 25ºC ern la cual se mide que cada 800cm3 contiene 60mg de
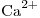 , 34mg de
, 34mg de 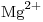 , 23mg de
, 23mg de 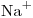 , 105mg de
, 105mg de  . 122mg de
. 122mg de 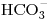 y 49mg de
y 49mg de 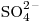 .
.- Calcular la dureza total, la dureza permanente y la dureza temporal. Explicar con ecuaciones a qué se le llama “Dureza temporal”.
- Proponga un método de ablandamiento, con sus respectivas ecuaciones.
Punto IV
- Escriba la ecuación de obtención, el tipo de polimerización, el monómero del cual se obtienen para los siguientes polímeros:
- Nylon 6,
- Teflón.
- Para los alumnos del 2007: (Había otro fragmento con un ejercicio de Ph para los alumnos del 2006, pero dado que esta era la última fecha de esos cursos, no lo transcribí.)
- Significado de orden de una reacción. Ejemplifique. Ecuación de Arrhesius: Definir todos sus términos.
- Predecir el signo de
 ,
,  y
y  a 1atm para:
a 1atm para:- Fusión del amoníaco a -60ºC,
- Fusión del amoníaco a -77.7ºC,
- Fusión del amoníaco a -100ºC.
- Era dato: Temperatura de fusión normal de
 = -77.7ºC
= -77.7ºC
Resolución
Discusión
Si ves algo que te parece incorrecto en la resolución y no te animás a cambiarlo, dejá tu comentario acá.